13일 미국 증권거래위원회에 따르면 2026년 5월 13일, 멀레큘린 바이오테크는 급성 골수성 백혈병(R/R AML) 치료를 위한 Annamycin과 cytarabine의 병용요법을 평가하는 주요 Phase 2B/3 "MIRACLE" 임상시험의 첫 데이터 공개가 임박했다고 발표했다.
이 임상시험은 Annamycin을 서로 다른 용량으로 투여하는 두 개의 팔과 cytarabine 및 위약을 포함하는 대조군으로 구성된다. 회사는 이 데이터 공개가 2026년 6월 30일 이전에 이루어질 것으로 예상하고 있다.
회사는 45명의 피험자에 대한 초기 블라인드 효능 데이터가 이전에 공개된 결과와 유사하게 나타나고 있으며, 복합 완전 관해율(CRc)이 40%를 초과하고, 완전 관해율(CR)은 약 30%에 달한다고 보고했다. 이러한 결과는 유사한 환자 집단에서 cytarabine 단독으로 관찰된 역사적 CR율인 약 17-18%와 비교할 때 긍정적인 결과이다. 현재 cytarabine은 AML의 2차 치료를 위한 승인된 표준 치료법이다.
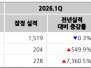
5월 1일 기준으로, MIRACLE 임상시험에는 총 56명의 피험자가 모집되어 있으며, 2026년 3분기까지 90명의 피험자를 모집할 계획이다. 회사의 회장 겸 CEO인 월터 클렘프는 "MIRACLE에서 나오는 데이터는 고무적이다"라고 말했다. "수십 년 동안 cytarabine 단독 요법은 재발 또는 불응성 AML에서 상대적으로 낮은 기준을 설정해 왔으며, 역사적 완전 관해율은 약 17-18%에 머물렀다.
MIRACLE 임상시험은 글로벌 다기관, 무작위, 이중 맹검, 위약 대조, 적응형 설계의 임상시험으로, 2B(Part A) 부분의 데이터는 Phase 3(Part B) 부분과 결합되어 주요 효능 지표를 측정할 예정이다. Part A는 Annamycin을 cytarabine과 병용하여 두 가지 용량(190 mg/m² 및 230 mg/m²)에서의 효과를 평가하도록 설계되었다.첫 번째 45명의 피험자에 대한 데이터 공개는 2026년 2분기 말에 이루어질 예정이다.
Annamycin은 현재 재발 또는 불응성 급성 골수성 백혈병 치료를 위해 FDA로부터 신속 승인 및 희귀의약품 지정을 받았으며, 2040년까지 물질 특허 보호를 받고 있다. 또한, 멀레큘린 바이오테크는 WP1066이라는 면역/전사 조절제를 개발 중이며, 이는 뇌종양, 췌장암 및 기타 암을 목표로 하고 있다. 회사는 현재 MIRACLE 임상시험을 통해 Annamycin과 cytarabine의 병용요법을 평가하고 있으며, 이 연구는 FDA와의 협의를 통해 개발 경로의 위험을 크게 줄였다.
현재 멀레큘린 바이오테크의 재무 상태는 안정적이며, 임상시험 진행을 위한 추가 자금 조달이 필요하다. 회사는 임상시험을 진행하기 위해 상당한 추가 자금이 필요하며, 이러한 자금 조달이 적시에 이루어질 수 있을지에 대한 불확실성이 존재한다.
※ 본 컨텐츠는 AI API를 이용하여 요약한 내용으로 수치나 문맥상 요약이 컨텐츠 원문과 다를 수 있습니다. 해당 컨텐츠는 투자 참고용이며 투자를 할때는 컨텐츠 원문을 필히 필독하시기 바랍니다.
데이터투자 공시팀 pr@datatooza.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
< 저작권자 ⓒ 데이터투자, 무단 전재 및 재배포 금지 >