12일 미국 증권거래위원회에 따르면 ARS파마슈티컬스는 2024년 8월 9일에 미국 식품의약국(FDA)으로부터 neffy(에피네프린 비강 스프레이)의 승인을 받았다.발표했다.
이는 체중이 30kg 이상인 성인 및 아동의 알레르기 반응(제1형 포함), 특히 아나필락시스를 응급 치료하기 위함이다.
이 승인은 2mg 용량의 에피네프린을 사용하는 다. 개의 주요 등록 연구에 기반하고 있으며, 해당 연구들은 여러 파일럿 및 보조 연구에 의해 지원되었다.
neffy는 정의된 모든 임상 목표를 충족했고, 약물 동태 및 약리 작용 데이터는 승인된 에피네프린 주사 제품 범위 내에 있었다.
연구 결과에 따르면, neffy의 임상 시험에서 부작용은 일반적으로 경미했고, 사용 시 비강 자극이나 통증 등의 의미 있는 부작용은 보고되지 않았다.neffy는 FDA 승인 후 8주 이내에 30kg 이상인 환자에게 제공될 예정이다.
또한, ARS파마슈티컬스는 2024년 3분기 말까지 15kg에서 30kg로 체중이 감소한 아동을 위한 neffy의 보충 NDA를 FDA에 제출할 계획이다.
유럽연합에서 neffy에 대한 마케팅 승인에 대한 긍정적인 의견이 2024년 6월 27일에 채택되었으며, EMA 결정은 일반적으로 CHMP 의견 채택 후 67일 이내에 내려진다.
이러한 승인이 이루어질 경우, 제약 회사는 2024년 4분기에 유럽에서 EURneffy를 환자에게 공급할 것으로 예상된다.
ARS파마슈티컬스의 혁신적인 제품인 neffy는 needle-free 방식으로 에피네프린을 전달하며, 환자들에게 사용자 친화적인 솔루션을 제공할 것으로 기대된다.
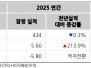
이 회사는 neffy의 마케팅 및 상용화 전략을 세우고 있으며, 해외 진출을 목표로 하고 있다.이와 관련하여 FDA와의 후속 연구 및 신청 계획도 수립 중에 있다.향후 3년 이상 지속 가능한 운영 기반을 제공할 것으로 보인다.ARS파마슈티컬스는 $218.7백만의 강력한 재무 구조를 보유하고 있으며, 서로 다.국가에서 neffy의 승인 및 상용화 기회를 모색하고 있다.
※ 본 컨텐츠는 AI API를 이용하여 요약한 내용으로 수치나 문맥상 요약이 컨텐츠 원문과 다를 수 있습니다. 해당 컨텐츠는 투자 참고용이며 투자를 할때는 컨텐츠 원문을 필히 필독하시기 바랍니다. 원문URL(https://www.sec.gov/Archives/edgar/data/1671858/000119312524198384/0001193125-24-198384-index.htm)
데이터투자 공시팀 pr@datatooza.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
< 저작권자 ⓒ 데이터투자, 무단 전재 및 재배포 금지 >