15일 미국 증권거래위원회에 따르면 2024년 8월 15일, 시가테크놀러지스는 "SIGA Statement on PALM 007 Topline Results in Mpox"라는 제목의 보도자료를 발표했다.보도자료의 전체 내용은 본 문서의 부록 99.1에 첨부되어 있으며, 여기서 참조된다.
보도자료에 따르면, PALM 007 연구의 초기 분석 결과, 연구는 모든 환자에 대한 병변 해결에서 테코비리마트가 위약보다 우수하다고 했다.주요 목표에 통계적 유의성을 달성하지 못했다.
그러나 결과는 테코비리마트가 조기 치료를 받은 환자와 중증 질환 환자에게 임상적 이점을 제공한다고 시사한다.
또한, 테코비리마트의 강력한 안전성 프로파일이 확인되었으며, mpox에 대한 테코비리마트의 추가 임상 시험이 계속 진행되고 있다.
미국 국립 알레르기 및 전염병 연구소(NIAID)는 PALM 007 임상 시험(NCT05559099)의 초기 분석 결과를 발표했다.
NIAID는 이 연구가 콩고 민주 공화국(DRC)에서 mpox 환자에게 시가의 테코비리마트를 투여한 결과, 28일 이내 병변 해결 시간에서 통계적으로 유의미한 개선을 달성하지 못했다고 보고했다.
모든 환자는 치료 기간 동안 입원 상태였으며, 이 연구는 미국 FDA의 임상 시험 신청 하에 수행된 등록 연구가 아니다.
테코비리마트를 투여받은 환자 중 증상이 무작위 배정 7일 이내에 시작된 환자와 WHO가 100개 이상의 피부 병변을 가진 중증 질환 환자에서 의미 있는 개선이 관찰되었다.
회사는 이러한 데이터가 조기 치료를 받는 환자와 중증 질환 환자에 대한 테코비리마트의 잠재적 이점을 평가하기 위한 추가 시험을 지원한다고 믿고 있다.
시가의 최고 과학 책임자인 데니스 흐루비는 "이 데이터는 조기 치료와 중증 질환 환자에서 최대의 이점을 보여주며, 이는 테코비리마트의 작용 메커니즘과 밀접하게 일치한다"고 말했다.또한, 이 연구에서 테코비리마트는 위약과 유사한 안전성 프로파일을 보였다.
이러한 결과는 건강한 자원봉사자를 대상으로 한 여러 이전 연구와 일치하며, 지난 15년 동안 테코비리마트에서 관찰된 강력한 안전성 프로파일을 더욱 뒷받침한다.
시가의 CEO인 디엠 응우옌은 "PALM 007 연구 결과에 매우 고무되어 있으며, 테코비리마트가 mpox 질환의 중증 환자와 조기 치료를 받은 환자에게 잠재적 이점을 제공한다고 보여주었다"고 말했다.
PALM 007 연구는 DRC 및 전 세계에서 발생한 2022년 mpox 발병에 대응하기 위한 글로벌 협력 이니셔티브의 일환으로 진행되었다.
이 연구는 다양한 질병 단계, 연령, 건강 상태의 환자가 시험에 참여할 수 있도록 설계되었다.
연구 데이터의 정확한 수집과 환자의 식사 접근을 보장하기 위해 모든 환자는 치료 기간 동안 입원 상태였으며, 이는 실제 mpox 환자에게는 제공되지 않는 수준의 치료를 받았다.
PALM 007에서 위약 그룹의 환자들은 DRC의 관찰 연구에서 사용된 결과보다 훨씬 더 유리한 결과를 보였으며, 이는 테코비리마트의 위약 대비 측정된 이점을 감소시킬 수 있었다.이 통제된 환경이 시험 결과에 미친 정확한 영향은 아직 알려지지 않았다.
전 세계의 시험 스폰서들이 추가 연구를 진행하고 있으며, 이는 회사가 mpox 환자에게 테코비리마트의 잠재적 이점을 더 깊이 이해하는 데 도움이 될 것으로 기대된다.
현재 STOMP(미국 및 기타 국가), UNITY(스위스, 브라질, 아르헨티나), Platinum-CAN(캐나다), EPOXI(유럽) 등 네 개의 무작위 임상 시험이 환자를 모집하고 있다.
PALM 007 연구와는 상당히 다른 점이 있는 이 연구들의 데이터는 시가가 PALM 007 결과가 시험 설계, 환자 집단, 의료 프로토콜, 질병 클레이드 또는 기타 변수에 의해 영향을 받았는지 이해하는 데 도움이 될 것이다.
응우옌 박사는 "모든 파트너와 환자, DRC에서 이 시험을 지원한 연구자들에게 감사드린다. 그들의 헌신과 공공 건강에 대한 기여는 테코비리마트에 대한 더 큰 이해를 얻는 데 중요한 역할을 했다"고 말했다.
PALM 007 연구는 mpox 바이러스 질환 치료를 위한 경구 테코비리마트의 안전성과 효능을 평가하기 위한 무작위, 위약 대조, 이중 맹검 시험이다.
참여 환자는 DRC에서 스크리닝 후 48시간 이내에 PCR 검사로 실험실에서 확인된 mpox 진단을 받았다.
환자는 3킬로그램(약 6.6파운드) 이상의 체중이 필요했으며, 나이에 대한 제한은 없었다.
환자는 14일 동안 경구 테코비리마트와 SOC 또는 위약과 SOC를 받기 위해 무작위(1:1)로 배정되었다.
테코비리마트를 받는 환자는 최소 2주 동안 입원하며, 28일 동안 추적 관찰되며, 장기 평가를 위한 선택적 방문이 59일째에 이루어진다.
효능의 주요 측정 기준은 모든 병변이 딱지가 생기거나 탈락되거나 새로운 표피층이 형성된 첫 번째 날까지의 일수이다.
시가테크놀러지스는 상업 단계의 제약 회사로, 감염병 치료 및 예방을 위한 혁신적인 의약품 개발에 주력하고 있다.
주요 제품인 TPOXX(테코비리마트)는 미국과 캐나다에서 천연두 치료를 위해 승인되었으며, 유럽과 영국에서는 천연두, mpox, 소천두 및 백신 부작용 치료를 위해 허가되었다.
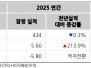
현재 시가의 재무 상태는 안정적이며, 향후 연구 결과에 따라 mpox 치료에 대한 테코비리마트의 잠재적 이점이 더욱 부각될 것으로 기대된다.
※ 본 컨텐츠는 AI API를 이용하여 요약한 내용으로 수치나 문맥상 요약이 컨텐츠 원문과 다를 수 있습니다. 해당 컨텐츠는 투자 참고용이며 투자를 할때는 컨텐츠 원문을 필히 필독하시기 바랍니다. 원문URL(https://www.sec.gov/Archives/edgar/data/1010086/000114036124037428/0001140361-24-037428-index.htm)
데이터투자 공시팀 pr@datatooza.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
< 저작권자 ⓒ 데이터투자, 무단 전재 및 재배포 금지 >