31일 미국 증권거래위원회에 따르면 2025년 3월 31일, 오메로스(Nasdaq: OMER)는 2024년 12월 31일로 종료된 4분기 및 연간 재무 결과를 발표했다.
2024년 4분기 순손실은 3,140만 달러, 주당 0.54 달러로, 2024년 3분기 순손실 3,220만 달러, 주당 0.56 달러와 비교된다.
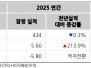
2024년 연간 순손실은 1억 5,680만 달러, 주당 2.70 달러로, 전년 동기 순손실 1억 1,780만 달러, 주당 1.88 달러에 비해 증가했다.
순손실의 변화는 OMIDRIA 계약 로열티 자산의 비현금 이익 재측정에서 3,320만 달러 감소, 이자 수익 660만 달러 감소, 2023년 12월 조기 채무 상환에서 410만 달러의 이익이 있었으나, 채무 매입 및 재융자에 따른 이자 비용 620만 달러 감소로 부분적으로 상쇄됐다.
2024년 12월 31일 기준으로, 오메로스는 운영 및 채무 서비스에 사용할 수 있는 현금 및 단기 투자 9,010만 달러를 보유하고 있으며, 이는 2023년 12월 31일 대비 8,170만 달러 감소한 수치이다.
연간 총 비용 지출은 4,270만 달러에 달하며, 이 중 2,170만 달러는 2026년 만기 전환 선순위 채권 매입과 관련된 지급, 1,910만 달러는 narsoplimab 약물 물질 배송 관련 비용, 190만 달러는 선순위 채권 거래 관련 비용이다.
오메로스는 이달 초, MASP-2를 표적으로 하는 항체 narsoplimab의 생물학적 라이센스 신청(BLA)을 FDA에 재제출했다.
재제출된 BLA에는 narsoplimab으로 치료받은 TA-TMA 환자와 외부 대조군의 생존율을 비교하는 프로토콜 및 통계 분석 계획의 결과가 포함되어 있다.
FDA의 PDUFA에 따른 조치 목표일은 재제출일로부터 6개월 후인 2025년 9월로 예상된다.유럽 마케팅 승인 신청(MAA)도 2025년 상반기에 제출할 예정이다.
오메로스는 zaltenibart의 3상 개발 프로그램을 시작했으며, 이는 PNH 환자를 대상으로 하는 연구를 포함한다.
오메로스의 CEO인 Gregory A. Demopulos는 "narsoplimab BLA가 FDA에 재제출되었으며, MAA는 분기에 제출될 예정이다"라고 밝혔다.
2024년 4분기 동안 OMIDRIA 로열티는 1,010만 달러로, Rayner의 미국 순매출 3,360만 달러에 해당한다.
2024년 4분기 총 운영 비용은 3,570만 달러로, 2024년 3분기 3,540만 달러와 비슷하다.2024년 4분기 이자 비용은 320만 달러로, 이전 분기 410만 달러에서 감소했다.
2024년 4분기 중단된 운영에서의 순이익은 520만 달러로, 이전 분기 490만 달러와 비교된다.
오메로스는 오늘 오후 1시 30분(태평양 표준시) 및 4시 30분(동부 표준시)에 재무 결과에 대한 컨퍼런스 콜을 개최할 예정이다.
오메로스의 현재 재무 상태는 순손실이 증가하고 있으며, 운영 비용이 지속적으로 발생하고 있는 상황이다.
※ 본 컨텐츠는 AI API를 이용하여 요약한 내용으로 수치나 문맥상 요약이 컨텐츠 원문과 다를 수 있습니다. 해당 컨텐츠는 투자 참고용이며 투자를 할때는 컨텐츠 원문을 필히 필독하시기 바랍니다. 원문URL(https://www.sec.gov/Archives/edgar/data/1285819/000143774925010211/0001437749-25-010211-index.htm)
데이터투자 공시팀 pr@datatooza.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
< 저작권자 ⓒ 데이터투자, 무단 전재 및 재배포 금지 >