- 미국 FDA 승인 획득 및 고형암 대상 안전성·효능 평가 착수
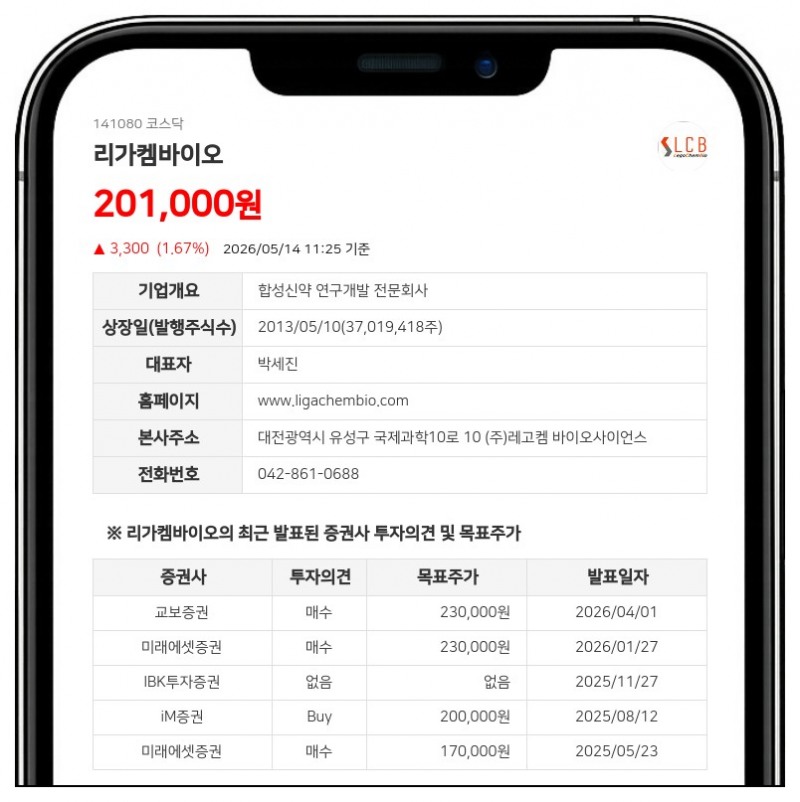
리가켐바이오는 2026년 5월 14일 미국 식품의약국(FDA)으로부터 CLDN18.2 표적 항체-약물 접합체(ADC) 후보물질인 LCB02A의 제1/2상 임상시험계획(IND)을 승인받았다고 공시했다.이번 임상시험은 CLDN18.2 양성 진행성 고형암 환자를 대상으로 LCB02A의 안전성과 내약성, 예비 효능을 평가하기 위한 최초 인체 대상 공개 및 다기관 연구로 진행될 예정이다.
주요 대상 질환은 위암과 위식도접합부암, 췌장암을 포함한 CLDN18.2 양성 고형암이며 한국과 미국, 캐나다 내 최대 20개 기관에서 임상시험을 실시할 계획인 것으로 확인됐다.
임상 1상 단계에서는 최대 8개 기관에서 용량 증량을 통해 안전성과 내약성을 확인하고 2상 투여 용량을 결정하며, 임상 2상 단계에서는 용량 확장을 통해 예비 효능을 집중적으로 평가한다.
임상시험의 1차 지표는 1상에서 용량제한 독성반응 발생 여부와 이상반응 빈도이며, 2상에서는 객관적 반응률(ORR)을 통해 신약 후보물질의 항종양 활성 효과를 직접적으로 확인하게 된다.
전체 목표 시험 대상자 수는 최대 191명으로 설정됐으며 임상시험 기간은 승인일로부터 약 60개월로 예상된다. 이에 따른 최종 임상 예상 종료일은 2031년 5월 14일로 예정되어 있다.
회사 측은 임상시험 약물이 의약품으로 최종 허가받을 확률은 통계적으로 약 10% 수준이며 임상 결과에 따라 상업화 계획이 변경되거나 포기될 가능성이 상존하므로 신중한 투자가 필요하다고 덧붙였다.
박승호 데이터투자 기자 shpark@datatooza.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
< 저작권자 ⓒ 데이터투자, 무단 전재 및 재배포 금지 >