14일 미국 증권거래위원회에 따르면 2026년 5월 14일, 리젠엑스바이오가 2026년 3월 31일로 종료된 분기의 재무 결과 및 운영 하이라이트를 발표했다.
회사는 RGX-202의 주요 Phase III AFFINITY DUCHENNE® 연구에서 긍정적인 주요 결과를 발표했으며, 주요 목표가 높은 통계적 유의성을 가지고 달성됐다.
RGX-202의 마이크로디스트로핀 발현과 기능적 개선 간의 통계적으로 유의미한 상관관계가 나타났으며, 이는 대체 목표의 유효성을 뒷받침한다.
또한, Surabgene lomparvovec (sura-vec, ABBV-RGX-314)는 당뇨병성 망막병증에 대한 주요 Phase IIb/III 연구를 위한 사이트가 활성화됐으며, 첫 환자 투여는 2026년 2분기로 예상된다.
RGX-121에 대한 임상 보류가 해제됐으며, 오늘 오전 8시(동부 표준시)에 RGX-202의 주요 데이터와 2026년 1분기 실적에 대해 논의하는 웹캐스트가 진행될 예정이다.
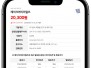
리젠엑스바이오의 2026년 3월 31일 기준 현금, 현금성 자산 및 시장성 증권은 150.5백만 달러로, 2025년 12월 31일 기준 240.9백만 달러에서 감소했다. 이 감소는 주로 2026년 1분기 운영 활동을 지원하기 위해 사용된 현금에 기인한다.
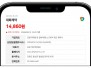
2026년 1분기 수익은 6.4백만 달러로, 2025년 1분기 89.0백만 달러에 비해 감소했다. 이 감소는 주로 2025년 1분기에 Nippon Shinyaku와의 협력에 따라 인식된 70.0백만 달러의 선급 라이센스 수익과 2026년 1월에 미국에서 라이센스 특허가 만료됨에 따라 ZOLGENSMA® 로열티 수익이 12.2백만 달러 감소한 데 기인한다.
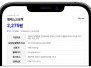
연구 및 개발 비용은 57.3백만 달러로, 2025년 1분기 53.1백만 달러에 비해 증가했다. 일반 및 관리 비용은 21.3백만 달러로, 2025년 1분기 20.3백만 달러에 비해 증가했다.
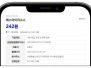
2026년 1분기 순손실은 90.1백만 달러로, 2025년 1분기 순이익 6.1백만 달러에 비해 큰 폭으로 감소했다.
리젠엑스바이오는 2026년 3월 31일 기준 150.5백만 달러의 현금 잔고가 2027년 초까지 운영을 지원할 것으로 예상하고 있으며, 이는 파트너나 라이센스 계약에 따른 개발 또는 규제 이정표 달성 시 발생할 수 있는 물질적 지급의 영향을 제외한 수치다.
또한, RGX-202의 긍정적인 주요 데이터와 안전성 프로필, 마이크로디스트로핀과 기능적 개선 간의 통계적으로 유의미한 상관관계를 바탕으로 리젠엑스바이오는 RGX-202의 가속 승인을 추진할 계획이다. 현재 리젠엑스바이오는 RGX-202의 상업적 출시를 2027년으로 준비하고 있다.
※ 본 컨텐츠는 AI API를 이용하여 요약한 내용으로 수치나 문맥상 요약이 컨텐츠 원문과 다를 수 있습니다. 해당 컨텐츠는 투자 참고용이며 투자를 할때는 컨텐츠 원문을 필히 필독하시기 바랍니다.
데이터투자 공시팀 pr@datatooza.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
< 저작권자 ⓒ 데이터투자, 무단 전재 및 재배포 금지 >